
TERMODINÁMICA – IRREVERSIBILIDAD
Cómo bien vimos en el artículo anterior, definimos los conceptos de termodinámica y la conservación de la energía. Recordando que la termodinámica trata las leyes que rigen la transformación de energía en un sistema, incluyendo de forma natural, el calor como energía. También recordamos que la termodinámica comprende los procesos térmicos, mecánicos, eléctricos y químicos.
En este artículo, nos concentraremos únicamente en la irreversibilidad en la termodinámica.
SEGUNDO PRINCIPIO DE LA TERMODINÁMICA.
IRREVERSIBILIDAD.
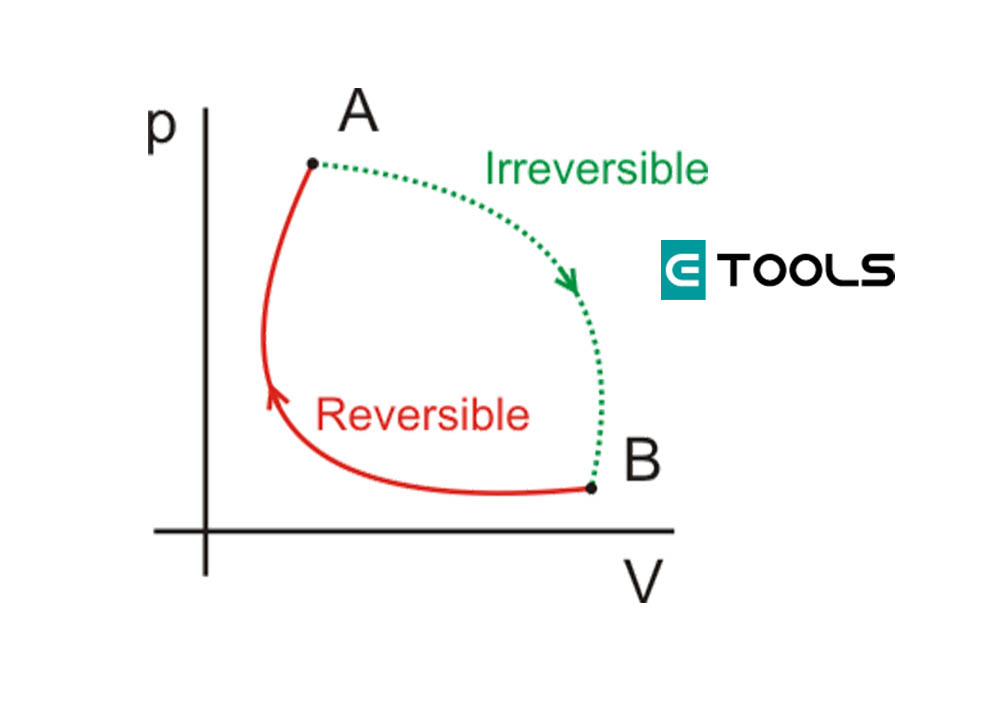
El calor fluye espontáneamente de una fuente caliente a otra fría. El proceso inverso nunca se produce espontáneamente en la naturaleza.
Esta transformación se denomine irreversible, por cuanto el sistema considerado no puede volver por sí mismo al estado primitivo, salo que se le entregue energía exterior.
Si un bloque se desliza sobre una superficie horizontal, la energía cinética del mismo se transforma en calor por rozamiento incrementando la energía interna del bloque y de la mesa, pero el proceso inverso, transformar ese calor en energía cinética no es posible.
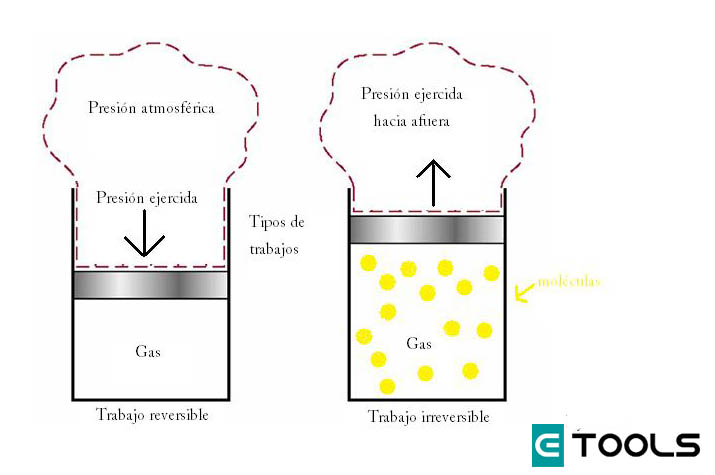
Es posible transformar trabajo mecánico en calor, pero es no es posible transformar el calor completamente en trabajo, si no se entrega al sistema energía del exterior. El primer principio de la termodinámica establece la equivalencia entre trabajo mecánico y calor, pero no indica en qué sentido se produce el proceso. De esto se ocupa el segundo principio de la termodinámica, que podemos enunciar así:
Es imposible que una máquina que realiza un ciclo de cerrado produzca una cantidad equivalente de trabajo mecánico quitando calor de una única fuente de calor.
Una máquina térmica de este tipo se denomina móvil perpetuo de segunda especie.
Lo expuesto es aplicable para obtener energía cinética. Para ello parte del calor extraído de la fuente caliente se transforma en energía mecánica y el resto se emplea en calentar una fuente más fría.
Si quieres conocer otros artículos parecidos a TERMODINÁMICA – IRREVERSIBILIDAD puedes visitar la categoría Fisica.





Deja un comentario