
EFECTO FOTOELÉCTRICO. DUALIDAD ONDA-CORPÚSCULO
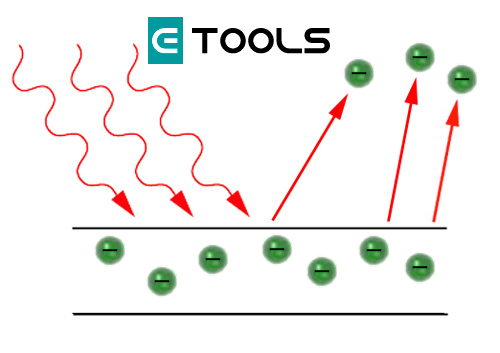
Cuando, en 1887, Heinrich Hertz descubrió que la superficie de un electrodo metálico en un tubo de vacío emitía electrones al ser iluminada, interpretó que la energía que suministra la radiación luminosa sirve para arrancar los electrones del metal y permitir el paso de corriente a través del tubo. Al considerar la luz como una onda, tal como había establecido Maxwell, el efecto fotoeléctrico se producía siempre que la intensidad luminosa fuera suficiente; y si aumentamos la frecuencia de la radiación incidente, aumenta la energía de los electrones emitidos.
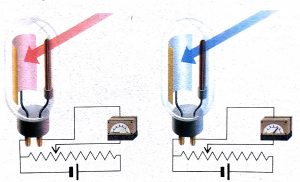
Experimentalmente se observó, sin embardo, que, para un metal determinado, sólo se detecta el paso de corriente si la luz tiene una frecuencia igual o superior al valor umbral (imagen). Para las frecuencias inferiores no se produce el fenómeno aunque se incremente la intensidad luminosa. Para radiaciones de frecuencia superior, la corriente aumenta con dicha intensidad luminosa.
Es posible que, para algunos materiales, una luz azul produzca efecto fotoeléctrico y no lo produzca una luz roja, aunque la intensidad de esta sea mayor.
Interpretación de Einstein
Los resultados experimentales sobre el efecto fotoeléctrico fueron explicados por Einstein en 1905, utilizando el concepto de quantum, introducido por Max Planck. Se reintroducía así la naturaleza corpuscular de la luz al suponerla formada por fotones individuales, a cada uno de los cuales le corresponde una energía E que depende de la frecuencia v: E = h.v1 en donde h es la constante de Planck, cuyo valor es 6,6 x 10-34 J·s.
Un electrón de haz que choca con un electrón de un átomo de la superficie, lo arranca sólo si su energía (es decir, su frecuencia) es suficiente. En caso contrario, para frecuencias inferiores, rebotará y, aunque aumente el número de fotones, éstos no arrancarán electrones y no circulará corriente, de acuerdo con los resultados experimentales. Un fotón con frecuencia v, superior a la frecuencia umbral v0 comunicará al electrón que arranque una energía cinética igual a la diferencia entre su energía (hv) y la mínima necesaria (hv0) o trabajo de extracción del electrón:
Rayos X
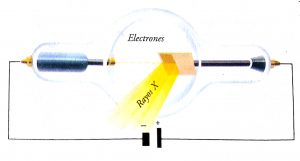
El fenómeno inverso al efecto fotoeléctrico es la generación de rayos X, descubierta por Wilhem Conrad Röntgen (1895) al observar la radiación emitida por un ánodo metálico al chocar los rayos catódicos sobre él (imagen). En 1912, Max von Laue comprobó que los rayos X tienen las mismas propiedades que la luz y sus frecuencias son mucho mayores, existiendo para cada metal un valor máximo V=. La energía cinética de los electrones que chocan con el anticátodo se libera en forma de rayos X, mientras no supere el valor de hvm.
Al chocar con el ánodo dispuesto e una manera especial (anticátodo), los electrones son absorbidos por el metal, pero arrancan de los átomos de éste fotones muy energéticos de rayos X. sus frecuencias son características del metal.
El efecto Compton
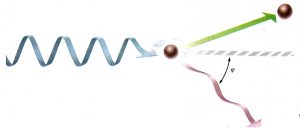
En 1923, Arthur H. Compton descubrió que si un fotón choca con un electrón, se comporta como un corpúsculo, de manera que las dos partículas se desvían como dos bolas elásticas que choquen: habrán intercambiado energía cinética y cantidad de movimiento. En efecto, la energía del fotón emitido después del choque es diferente de la del incidente, pues, como se puede comprobar, lo son sus frecuencias respectivas. El electrón recibe una energía cinética igual a la diferencia entre la energía del fotón incidente y la del dispersado.
Efecto Compton. La energía que el fotón incidente comunica al electrón está relacionada al ángulo de dispersión. El fotón emergente tiene una longitud de onda mayor.
Dualidad onda-corpúsculo
La teoría ondulatoria clásica explica los fenómenos de propagación de la luz, interferencias, difracción, polarización, etc. Sin embargo, los fenómenos descritos en este artículo confieren a la luz un comportamiento corpuscular. Debemos admitir que la luz posee una doble naturaleza, ondulatoria y corpuscular, aspectos que se complementan entre sí y que aparecen como formas distintas de percibir una realidad.
Los electrones que inciden sobre palas hacen que gire el molino: los electrones tienen propiedades corpusculares.
En 1924, Louis de Broflie amplió este razonamiento a las partículas consideradas hasta entonces como materiales: la materia debe tener también un comportamiento ondulatorio que se pondrá de manifiesto siempre que se realicen los experimentos en las condiciones adecuadas. Pocos años después se comprobaba la dispersión sufrida por un haz de electrones al chocar con la red formada por los átomos de un cristal, experiencia en todo análoga a la dispersión de la luz. Todo cuerpo material tiene una onda asociada, cuya longitud de onda (λ) corresponde al cociente entre h (constante de Planck) y p (cantidad de movimiento = m . v). Las características ondulatorias solamente tienen importancia para partículas atómicas.
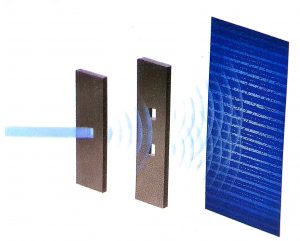
Cuando un haz de electrones atraviesa las dos rendijas de un dispositivo como el de la figura, aparecen franjas de difracción: los electrones tiene propiedades ondulatorias.
La adscripción de un comportamiento ondulatorio a la materia y su coexistencia con la idea de corpúsculo nos impide utilizar imágenes conocidas para comprender la realidad. Debemos recurrir a descripciones más abstractas, limitándonos a dar los valores de las propiedades conocidas y admitiendo que algunas de las propiedades del mundo macroscópico son improcedentes en el mundo de las partículas.
¡Si te gustó este artículo no dudes en dejarnos tus comentarios o consultas aquí abajo!
Si quieres conocer otros artículos parecidos a EFECTO FOTOELÉCTRICO. DUALIDAD ONDA-CORPÚSCULO puedes visitar la categoría Fisica.






Deja un comentario